ÉQUIPE 5 – Fabienne Foufelle – Maladies métaboliques, diabète et comorbidités

L’équipe « Maladies métaboliques, diabète et comorbidités » (MEDICIS) a trois objectifs : (i) l’étude des comorbidités du diabète de type 2, telles que la résistance à l’insuline et la stéatose hépatique non alcoolique, ainsi que leur relation avec le métabolisme lipidique; (ii) le rôle du récepteur des minéralocorticoïdes dans les maladies cardiométaboliques et cardiorénales; (iii) les mécanismes du remodelage cardiaque au cours du vieillissement.
Le groupe dirigé par F. Foufelle étudie la relation complexe entre la « maladie hépatique stéatosique associée à un dysfonctionnement métabolique » (MASLD) et le diabète de type 2, ainsi que les mécanismes de la résistance à l’insuline induite par les lipides, caractéristique majeure du diabète de type 2. Il s’intéresse particulièrement : (i) au rôle multifactoriel des mitochondries dans la progression de la MASLD et de la fibrose hépatique; (ii) au rôle des espèces de sphingolipides (céramides, dihydrocéramides et sphingosine-1-phosphate) dans le métabolisme hépatique et la résistance à l’insuline; (iii) au rôle du stress du réticulum endoplasmique dans la stéatohépatite associée à un dysfonctionnement métabolique (MASH).
Il existe une forte continuité entre recherche fondamentale et clinique, grâce à la présence conjointe de chercheurs et de cliniciens (services de diabétologie et d’hépatologie de l’hôpital de la Pitié-Salpêtrière).
Le groupe dirigé par F. Jaisser se concentre sur la compréhension des rôles de signalisation et des rôles physiopathologiques de l’hormone aldostérone et de son récepteur, le récepteur des minéralocorticoïdes (MR), avec pour objectif principal la traduction des données précliniques vers des études cliniques, incluant le développement d’essais cliniques interventionnels lorsque cela est possible. Le groupe a développé plusieurs modèles de rongeurs et de porcs afin d’évaluer les rôles du MR et de ses cibles en aval dans les domaines rénal et cardiovasculaire, ainsi qu’au-delà (foie, rétine, peau et tissu adipeux, par exemple). De nouvelles cibles en aval du MR, telles que la lipocaline associée à la gélatinase des neutrophiles (NGAL), ont été identifiées et leur rôle est actuellement étudié, notamment dans la MASLD. Le repositionnement des antagonistes du MR est étudié dans le cadre de recherches translationnelles majeures en collaboration avec plusieurs entreprises pharmaceutiques.
S. Besse étudie les mécanismes responsables de la transition vers l’insuffisance cardiaque au cours du vieillissement, en particulier les voies de signalisation NF-κB et FoxO dans le cœur de rongeur et humain.
 Quatre axes principaux sont développés :
Quatre axes principaux sont développés :
1- Sphingolipides et résistance à l’insuline
2- Dialogue inter-organes dans les pathologies métaboliques
3- Mécanismes cellulaires et moléculaires de la stéatose et de la stéatohépatite
4- Cœur, rein et minéralocorticoïdes
THEME 1. Sphingolipides et résistance à l’insuline

Eric HAJDUCH
La résistance à l’insuline est une condition pathologique dans laquelle les organes sensibles à l’insuline — le foie, les muscles et le tissu adipeux — ne répondent plus correctement à l’action de l’insuline, une hormone produite par les cellules β du pancréas.
Normalement, l’insuline facilite l’entrée du glucose dans les cellules musculaires et adipeuses, inhibe la production hépatique de glucose et favorise le stockage des lipides dans le tissu adipeux tout en ralentissant leur dégradation (lipolyse).
En cas de résistance à l’insuline, les cellules ne répondent plus efficacement à l’hormone : la glycémie reste élevée (hyperglycémie) et le pancréas compense par une hyperinsulinémie (surproduction d’insuline), ce qui peut conduire à l’épuisement progressif des cellules β pancréatiques. Les conséquences métaboliques possibles incluent une hyperglycémie chronique, une hyperinsulinémie, une stéatose hépatique, une dyslipidémie, une hypertension artérielle et le développement potentiel d’un diabète de type 2 (DT2).
Les facteurs contribuant à la résistance à l’insuline comprennent le surpoids et l’obésité abdominale, la sédentarité, une alimentation riche en sucres simples et en graisses saturées, l’inflammation chronique et un déséquilibre du microbiote intestinal.
Dans le contexte de l’obésité, principal facteur de risque du DT2, des tissus non adipeux tels que le muscle squelettique et le foie accumulent des lipides, parmi lesquels des dérivés des sphingolipides comme les céramides. Les céramides comptent parmi les messagers lipidiques les plus actifs pour inhiber des protéines clés de la voie de signalisation de l’insuline, induisant ainsi une résistance à l’insuline dans ces tissus.
Nos objectifs sont de comprendre les mécanismes par lesquels les sphingolipides produits par les foies stéatosiques influencent le métabolisme périphérique.
Nous étudions les céramides associés aux lipoprotéines circulantes dans le sang, dont les concentrations augmentent significativement dans les situations de MASLD. Certaines études ont montré que les céramides associés aux LDL (lipoprotéines de basse densité) peuvent exercer des effets délétères sur le métabolisme musculaire. Nous souhaitons caractériser les espèces de céramides impliquées (par exemple chaînes courtes ou longues) ainsi que les mécanismes en jeu (rôle du récepteur des LDL, métabolisme cellulaire des céramides…), à travers des études in vivo et in vitro (myotubes en culture).
Si le rôle des céramides dans le développement de la résistance à l’insuline et des maladies cardiovasculaires est désormais bien établi, celui d’un autre sphingolipide, la sphingosine-1-phosphate (S1P), reste encore mal élucidé. La S1P est produite par le foie et par les plaquettes et est associée aux HDL (lipoprotéines de haute densité) ou à l’albumine.
L’obésité et le diabète sont associés à une augmentation des concentrations de LDL contenant des céramides, mais également à une diminution des concentrations de HDL-S1P. Il a été montré que la HDL-S1P favorise la fonction et la survie des cellules β pancréatiques et pourrait également améliorer la signalisation de l’insuline. La résistance à l’insuline induite par l’obésité réduit les niveaux de HDL-S1P.
Notre projet vise à comprendre l’implication de ce sphingolipide dans les maladies métaboliques (MASLD, obésité, diabète) ainsi que les mécanismes sous-jacents chez la souris et chez l’Homme.
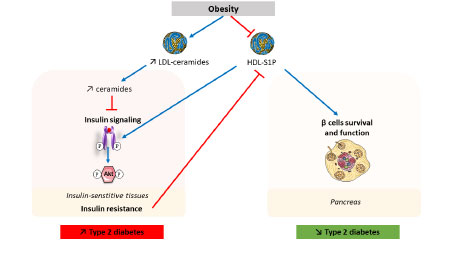
Implication des sphingolipides dans le diabète de type 2
THEME 2. Dialogue inter-organes dans les pathologies métaboliques

Franck Phan et Olivier Bourron
Les maladies métaboliques chroniques, telles que l’obésité et le diabète de type 2 (DT2), connaissent une augmentation rapide à l’échelle mondiale. Elles sont fréquemment associées à la MASLD (maladie hépatique stéatosique associée à un dysfonctionnement métabolique), reflétant l’implication du foie dans le syndrome métabolique. Ces trois affections sont étroitement liées : l’obésité et le DT2 constituent des facteurs de risque majeurs du développement de la MASLD, tandis que la progression de la MASLD peut, en retour, aggraver l’homéostasie métabolique globale.
Lorsqu’il n’est pas correctement pris en charge, le DT2 peut entraîner des complications chroniques, notamment cardiovasculaires et neurologiques périphériques, qui altèrent sévèrement la qualité de vie des patients et aggravent leur pronostic.
Loin de résulter de dysfonctionnements métaboliques isolés, ces maladies reposent sur une physiopathologie systémique et intégrée qui dépasse les « organes métaboliques classiques » tels que le foie, le tissu adipeux ou le muscle. En effet, ces pathologies s’accompagnent d’un déséquilibre complexe des échanges inter-organes, médiés par une grande variété de signaux bioactifs — lipides, cytokines, métabolites et peptides hormonaux — qui orchestrent un dialogue inter-tissulaire pathologique.
Comprendre les mécanismes moléculaires et cellulaires qui régissent ces interactions inter-organes constitue un enjeu majeur pour identifier de nouvelles cibles thérapeutiques et concevoir des approches plus intégrées pour la prévention et le traitement des maladies métaboliques et de leurs complications.
Notre programme de recherche s’inscrit dans cette approche systémique, en explorant les interactions fonctionnelles entre le foie, le tissu adipeux, le cœur ainsi que les systèmes artériel et nerveux périphérique dans le contexte de perturbations métaboliques telles que la MASLD, le diabète de type 2 et l’obésité.
L’originalité de notre démarche réside dans sa forte intégration entre recherche fondamentale, modélisation expérimentale et investigation clinique, avec un engagement clair vers une traduction rapide en pratique clinique.
Grâce à l’utilisation de technologies de pointe — telles que la lipidomique, la métabolomique, la transcriptomique et les études physiologiques fonctionnelles — ainsi qu’à la disponibilité de cohortes humaines, nos travaux visent à décrypter comment les signaux émis par un organe altéré (comme un foie stéatosique ou un tissu adipeux inflammatoire) peuvent déclencher des réponses pathologiques dans d’autres tissus, notamment le cœur, les artères et le système nerveux périphérique, contribuant ainsi au développement et à l’aggravation des complications associées au syndrome métabolique et au diabète.
Parmi nos projets majeurs :
- Le projet NADRANK vise à mieux comprendre les échanges moléculaires entre le tissu adipeux et le foie et leur impact sur le développement et la progression de la MASLD ainsi que sur ses complications systémiques.
- Le projet CONNECT explore le lien entre atteinte hépatique et dysfonction cardiaque dans la MASLD, à travers l’étude de molécules de signalisation circulantes d’origine hépatique capables de moduler l’inflammation, la fibrose ou le remodelage myocardique.
- Le projet SYNAPSE étudie les mécanismes moléculaires sous-jacents aux neuropathies périphériques chez les patients atteints de MASLD et/ou de diabète de type 2, afin de mieux comprendre cette complication fréquente pour laquelle il n’existe actuellement aucun traitement curatif.
L’ensemble de ces projets repose sur une forte structuration hospitalo-universitaire, en collaboration étroite avec les services cliniques de l’hôpital de la Pitié-Salpêtrière – APHP (diabétologie, hépatologie, cardiologie) ainsi qu’avec les plateformes techniques de Sorbonne Université et de l’INSERM.
Notre capacité à relier les niveaux moléculaire, tissulaire et clinique dans une vision systémique des maladies métaboliques constitue une valeur ajoutée majeure pour la réussite de notre programme de recherche.
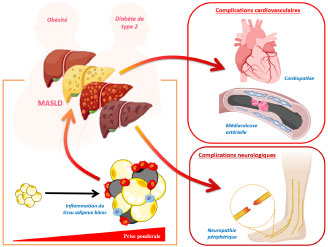
Interactions inter-organes et complications systémiques dans les maladies métaboliques : focus sur le tissu adipeux, le foie, le cœur et le système nerveux périphérique
THEME 3. Mécanismes cellulaires et moléculaires de la stéatose et de la stéatohépatite

Fabienne Foufelle Marie Lagouge
La maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD) est une pathologie hépatique dont l’incidence augmente régulièrement à l’échelle mondiale. La MASLD est une comorbidité fortement associée au diabète de type 2 et à l’obésité. Sa prévalence est estimée à 30 % dans la population générale et à plus de 80 % chez les personnes obèses.
La MASLD regroupe un spectre de pathologies allant de la stéatose simple, caractérisée par une accumulation de lipides dans les hépatocytes, à la stéatohépatite associée à un dysfonctionnement métabolique (MASH), dont les principales caractéristiques sont l’inflammation et la fibrose. La fibrose peut évoluer vers des pathologies plus sévères telles que la cirrhose et le carcinome hépatocellulaire (CHC), et elle est également fortement associée aux maladies cardiovasculaires.
Notre équipe possède une expertise approfondie dans l’étude des maladies hépatiques associées au diabète de type 2, en particulier les aspects de la stéatose liés au métabolisme lipidique.
Ces dernières années, nos projets se sont concentrés sur l’étude de la progression de la stéatose vers des stades plus sévères de la MASLD, tels que la MASH. Nous nous intéressons particulièrement aux mécanismes cellulaires et moléculaires qui contrôlent l’activité des différents types cellulaires du foie, notamment les hépatocytes — cellules prédominantes et acteurs métaboliques clés du foie — ainsi que les cellules stellaires hépatiques, responsables de la fibrogenèse.
Nos recherches portent plus particulièrement sur le métabolisme lipidique de ces cellules en lien avec l’activité du réticulum endoplasmique et des mitochondries.
Nos principaux projets actuels sont :
- Le projet IRE1 NASH (en cours d’achèvement) ;
- Le projet IMHOTEP, qui étudie le rôle du dysfonctionnement mitochondrial des hépatocytes dans l’initiation et la progression de la MASLD ;
- Les projets MITOSTAR et CEMPR, qui explorent respectivement le rôle de l’activité mitochondriale dans la transdifférenciation des cellules stellaires hépatiques et la fibrogenèse hépatique, ainsi que l’importance des contacts entre le réticulum endoplasmique et les mitochondries dans les cellules stellaires hépatiques au cours de la progression et de la régression de la MASLD.
L’ensemble de ces travaux combine des études physiologiques sur des modèles précliniques et des explorations cellulaires et moléculaires, nous permettant d’approfondir nos connaissances sur le rôle joué par les organites intracellulaires (réticulum endoplasmique et mitochondries) dans l’initiation et la progression de la MASLD.
.
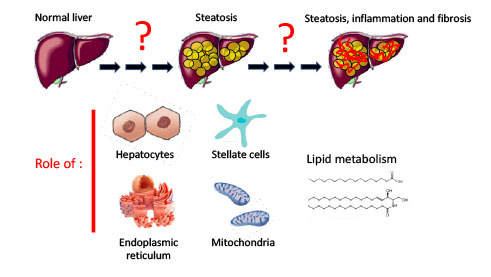
Quels sont les acteurs et les mécanismes de la MASLD/MASH ?
THEME 4. Cœur, rein et minéralocorticoïdes

Fréderic JAISSER et Sophie BESSE
Notre objectif est d’améliorer la compréhension du rôle physiopathologique des voies de signalisation par lesquelles le vieillissement cardiaque et le récepteur des minéralocorticoïdes (MR) favorisent les pathologies cardiaques dans le contexte des maladies métaboliques et rénales.
Nos travaux combinent des approches cellulaires et moléculaires, des études de physiologie animale ainsi que des investigations pharmacologiques. Ils incluent également une dimension translationnelle visant à identifier et valider chez l’Homme les voies de signalisation mises en évidence dans les modèles cellulaires ou animaux.
Notre objectif est aussi de renforcer les bases scientifiques justifiant le développement de nouvelles applications thérapeutiques des antagonistes du récepteur des minéralocorticoïdes. Nous cherchons notamment à comprendre les mécanismes responsables du remodelage cardiaque au cours du vieillissement.
Dans un modèle de tissu atrial humain, nous explorons la contribution relative des différentes voies de mort cellulaire et de leurs mécanismes de régulation, conduisant à l’épuisement du pool de cardiomyocytes viables avec l’âge et au remodelage de la matrice extracellulaire.
Un deuxième axe de recherche concerne l’implication du MR dans le syndrome cardiorénal, en particulier dans l’insuffisance cardiaque à fraction d’éjection préservée et les valvulopathies aortiques, deux pathologies associées à la maladie rénale chronique. Nous avons identifié la lipocaline associée à la gélatinase des neutrophiles (NGAL) comme une cible en aval du MR, dont le rôle est déterminant dans les effets délétères de l’activation du MR dans ces pathologies.
Un troisième axe, mené en collaboration, explore le rôle du MR dans diverses pathologies extrarénales ou extracardiaques, par exemple en ophtalmologie, dans les maladies inflammatoires chroniques de l’intestin ou encore au niveau de la cavité buccale.
Enfin, plusieurs partenariats ont été établis avec de grandes entreprises pharmaceutiques afin de caractériser de nouveaux antagonistes non stéroïdiens du MR et d’évaluer leurs bénéfices dans différentes comorbidités.
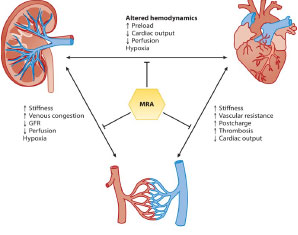
Effets bénéfiques des antagonistes du récepteur des minéralocorticoïdes (MRA) en néphro-cardiologie

| Name | Position | ORCID |
|---|
- Le Goff W, BOURRON O, Materne C, Galier S, PHAN F, Tan-Chen S, Guillas I, HARTEMANN A, Salem JE, Redheuil A, FOUFELLE F, Le Stunff H, HAJDUCH E, Guerin M. Inverse relationship between circulating sphingosine-1-phosphate and precursor species and coronary artery calcification score in type 2 diabetes. Cardiovasc Diabetol. 2025 Feb 21;24(1):85.
- DENIMAL D, Ponnaiah M, PHAN F, Jeannin AC, Redheuil A, Salem JE, Boussouar S, Paulstephenraj P, Laroche S, Amouyal C, HARTEMANN A, FOUFELLE F, BOURRON O. Metabolic dysfunction-associated steatotic liver disease (MASLD) biomarkers and progression of lower limb arterial calcification in patients with type 2 diabetes: a prospective cohort study. Cardiovasc Diabetol. 2025 Apr 23;24(1):176.
- JAISSER F, BARRERA-CHIMAL J. Mineralocorticoid receptor antagonism for non-diabetic kidney disease. Nephrol Dial Transplant. 2025 Feb 5;40:i29-i36.
- Harrison SA, Bedossa P, Guy CD, Schattenberg JM, Loomba R, Taub R, Labriola D, Moussa SE, Neff GW, Rinella ME, Anstee QM, Abdelmalek MF, Younossi Z, Baum SJ, Francque S, Charlton MR, Newsome PN, Lanthier N, Schiefke I, Mangia A, Pericàs JM, Patil R, Sanyal AJ, Noureddin M, Bansal MB, Alkhouri N, Castera L, Rudraraju M, RATZIU V; MAESTRO-NASH Investigators. A Phase 3, Randomized, Controlled Trial of Resmetirom in NASH with Liver Fibrosis. N Engl J Med. 2024 Feb 8;390(6):497-509.
- BONNARD B, El Moghrabi S, Ueda K, Lattenist L, Soulie M, López-Andrés N, Xhaard C, Shimosawa T, Rossignol P, JAISSER F. NGAL is a Novel Target in Hypertension by Modulating the NCC-Mediated Renal Na Balance. Hypertension. 2023 Sep;80(9):1860-1870.
- Bandet CL, Tan-Chen S, Ali-Berrada S, Campana M, Poirier M, Blachnio-Zabielska A, Pais-de-Barros JP, Rouch C, Ferré P, Foufelle F, Le Stunff H, Hajduch E. Ceramide analog C2-cer induces a loss in insulin sensitivity in muscle cells through the salvage/recycling pathway. J Biol Chem. 2023 Jun;299(6):104815.
- HAJDUCH E, LACHKAR F, FERRE P, FOUFELLE F. Roles of Ceramides in Non-Alcoholic Fatty Liver Disease. J Clin Med. 2021 Feb 16;10(4):792.
- CARLIER A, PHAN F, SZPIGEL A, HAJDUCH E, Salem JE, Gautheron J, Le Goff W, Guérin M, LACHKAR F, RATZIU V, HARTEMANN A, FERRE P, FOUFELLE F, BOURRON O. Dihydroceramides in Triglyceride-Enriched VLDL Are Associated with Nonalcoholic Fatty Liver Disease Severity in Type 2 Diabetes. Cell Rep Med. 2020 Dec 22;1(9):100154.
- BOURRON O, PHAN F, Diallo MH, Hajage D, Aubert CE, CARLIER A, Salem JE, Funck-Brentano C, Kemel S, Cluzel P, Redheuil A, DAVAINE JM, Massy Z, Mentaverri R, Bonnefont-Rousselot D, Gillery P, Jaisson S, Vermeer C, Lacorte JM, Bouziri N, Laroche S, Amouyal C, HARTEMAN A. Circulating Receptor Activator of Nuclear Factor kB Ligand and triglycerides are associated with progression of lower limb arterial calcification in type 2 diabetes: a prospective, observational cohort study. Cardiovasc Diabetol 2020 Sep 18;19(1):140.
- BANDET CL, MAHFOUZ R, Véret J, Sotiropoulos A, POIRIER M, Giussani P, Campana M, Philippe E, Blachnio-Zabielska A, BALLAIRE R, LE LIEPVRE X, BOURRON O, Berkeš D, Górski J, FERRE P, Le Stunff H, FOUFELLE F, HAJDUCH E. Ceramide Transporter CERT Is Involved in Muscle Insulin Signaling Defects Under Lipotoxic Conditions. Diabetes. 2018 Jul;67(7):1258-1271.
- Besse S, Nadaud S, Balse E, Pavoine C. Early Protective Role of Inflammation in Cardiac Remodeling and Heart Failure: Focus on TNFα and Resident Macrophages.
Cells. 2022, 11(7):1249.
 |
Université Paris Saclay, Université Paris Cité, Université Côte d’Azur, Université de Dijon, Université de Lorraine, CIC CHU Nancy Brabois, Université de Compiègne, Université de Rouen. |
 |
Bialystok University, Poland; Universidad de Valladolid, Spain; Universidad Pública de Navarra, Pamplona, Spain; DZHK (German Centres for Cardiovascular Research). |
 |
Melbourne University, Australia; Augusta University, USA; Université de Montréal, Canada; San Sebastián University, Chile. |
 |
Bayer SAS, AstraZeneca, Poxel, Enterome. |
The team is a member of the IHU “ICAN” and the Fédération Hospitalo-Universitaire – Groupe Transplantation Ile De France
- Frédéric JAISSER Inhibitors of NGAL protein WO 2020/1784412019 INSERM, Université de Rouen Normandie, Greenpharma S.A.S, Sorbonne Université, UNIVERSITE DE PARIS
- Olivier BOURRON, Agnès HARTEMANN Method for diagnosis and treating peripheral neuropathies Brevet Europe EP 18306503.6 2018 Sorbonne Université Pr. Bourron is the laureate of the 2020 innov APHP trophy



